本文转载自口腔科普网公众号,原文链接:https://mp.weixin.qq.com/s/9UJtjzVSzgTwklwN3U7-Hg
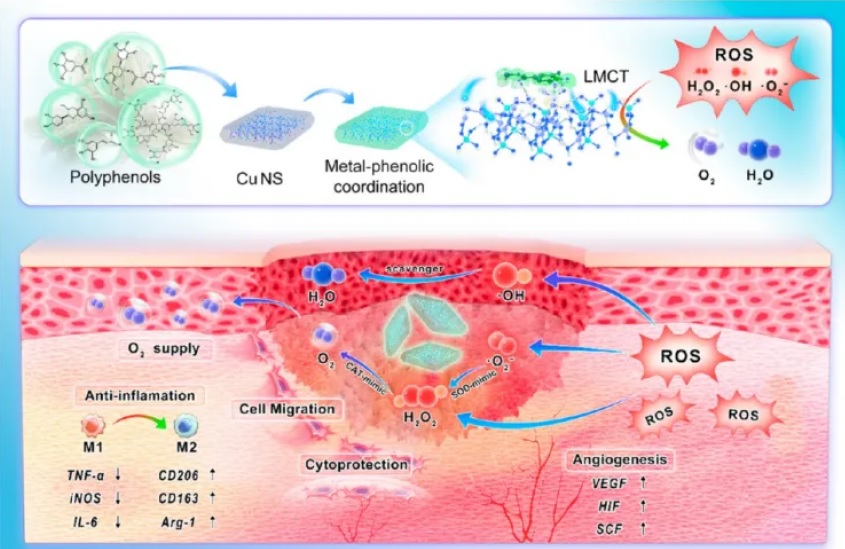
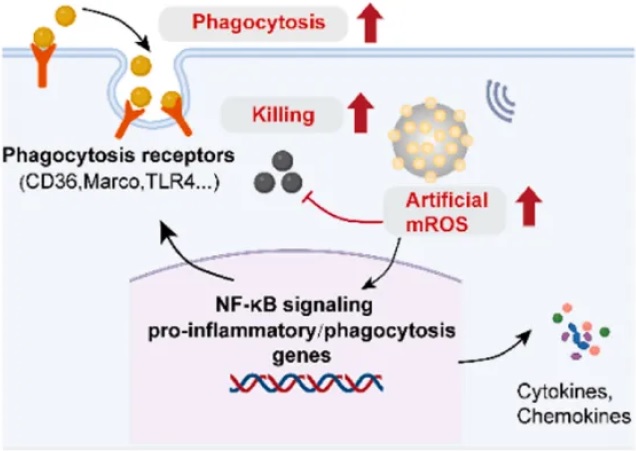
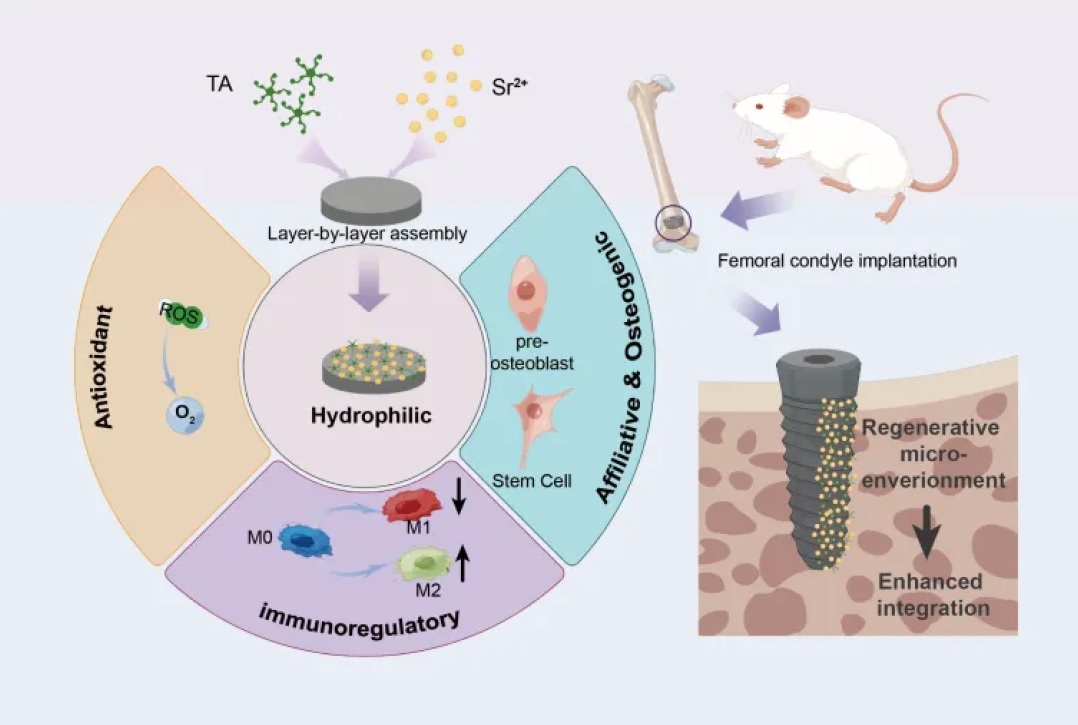
近日,山东大学口腔医学院(口腔医院)葛少华教授、李建华教授口腔生物材料研究团队,围绕口腔感染和组织再生临床问题,在基于金属多酚配位网络的生物活性界面研究方面取得系列新进展,成果分别发表在《纳米科学与技术》ACS Nano(IF=17.1)、《纳米能源研究》Nano Energy(IF=17.5)、《先进科学》Advanced Science (IF=16.7),山东大学口腔医学院均为第一完成单位。进展一:发现多酚配体-金属电荷转移具有界面类酶催化行为,用于慢性伤口愈合慢性伤口是糖尿病的一种常见并发症,可导致感染、截肢、残疾,甚至死亡等严重后果,对人类健康危害严重。身体长期处于高血糖状态导致伤口组织活性氧(ROS)增加,氧化还原平衡被破坏从而加剧了炎症反应,伤口修复过程所必需的细胞血管生成和迁移等功能也被损害,最终阻碍伤口愈合。该团队提出了一种由多酚配体-金属电荷转移(LMCT)诱导的2D铜抗氧化纳米酶,该纳米酶由单宁酸TA和磷酸铜纳米片化学配位形成,以消除ROS并促进慢性糖尿病伤口愈合。该研究发现,铜纳米片上配位的多酚配体会使界面处具有较强的电荷转移能力,并能调节Cu的价态,TA配位还可以减轻直接使用Cu纳米材料的细胞毒性作用。同时该纳米酶对不同的氧化物种表现出有效的清除能力,通过分解ROS保护细胞免受氧化损伤,并能通过促进上皮再生、胶原沉积、血管生成和免疫调节来促进糖尿病伤口的愈合。这项工作证明了基于多酚配体的LMCT在纳米界面上诱导的类酶清除ROS能力,为构建用于治疗糖尿病伤口和其他疾病的金属基纳米酶提供了一种新的策略。相关研究成果以“多酚配体-金属电荷转移诱导具有清除活性氧簇能力的铜纳米酶用于慢性伤口愈合(Phenolic Ligand-Metal Charge Transfer Induced Copper Nanozyme with Reactive Oxygen Species-Scavenging Ability for Chronic Wound Healing)”为题,发表在国际期刊ACS Nano上,葛少华教授、李建华教授为共同通讯作者,山东大学口腔医学院(医院)博士生陈意为第一作者。进展二:金属多酚配位界面介导胞内递送纳米压电催化,构建mROS启发的工程化巨噬细胞,用于感染清除每年全球约数百万人死于细菌感染,其中因金黄色葡萄球菌(S. aureus)感染死亡的占比最大,可引起败血症、肺炎、皮肤软组织感染等疾病。现有传统的治疗金葡菌感染的方法包括物理清除和抗生素治疗,这可能导致清除不彻底、清除过度损伤组织或出现耐药性。巨噬细胞等人类先天免疫细胞是宿主抵御细菌感染的第一道防线,线粒体活性氧(mROS)在巨噬细胞的免疫反应中起重要作用。然而, S. aureus已经进化出抑制mROS生成等多种逃避免疫系统攻击的防御策略,使细菌长期在体内存活。该团队提出了具有人工mROS生成能力的纳米压电工程化巨噬细胞的概念。这一概念通过金属多酚网络(MPN)介导的溶酶体逃逸和增强的细胞内压电催化实现。MPN是一种由多酚配体和金属离子自组装形成的超分子网络,具有电荷和质子缓冲能力,可以在进入细胞之前阻断纳米压电的ROS产生,确保其脱靶生物安全性。当被巨噬细胞内化后,MPN可以在溶酶体内诱导质子“海绵效应”,从而通过溶酶体逃逸将纳米压电催化输送到细胞质。在超声条件下,压电工程化巨噬细胞表现出对S. aureus增强的吞噬作用和较强的杀菌活性。通过靶向配体修饰的纳米压电纳米颗粒在感染部位原位工程化巨噬细胞,对S. aureus脓肿感染模型中展现出来较好的治疗效果。这项研究揭示了细胞内压电纳米催化在增强巨噬细胞先天免疫反应方面的潜力,为巨噬细胞介导的免疫疗法提供了一种非侵入性治疗思路。相关研究成果以“细胞内传递压电主导的纳米催化,来模拟线粒体ROS生成,为巨噬细胞免疫治疗提供动力(Intracellular delivery of piezotronic-dominated nanocatalysis to mimic mitochondrial ROS generation for powering macrophage immunotherapy)”为题,发表在国际期刊Nano Energy 上,葛少华教授、李建华教授、刘宏教授为共同通讯作者,山东大学口腔医学院(医院)硕士生冯俊昆为第一作者。进展三:金属多酚配位界面调节早期免疫,增强口腔钛种植体骨整合针对口腔种植修复过程中种植体植入后异常免疫应答导致骨结合不良问题,该团队成功在医用钛合金表面原位构建了多酚-锶(TA-Sr)配位多功能纳米涂层。该涂层具有良好的表面适应性、生物相容性、亲水性以及优异的自由基清除能力,并能持续释放Sr2+促进成骨分化并诱导矿化形成更多骨质较佳的新骨,增强种植体与宿主骨结合效果。同时该研究发现含有TA-Sr涂层的种植体植入后可调控巨噬细胞,抑制其向M1型极化并诱导M2型极化,这种在种植早期对周围免疫微环境的调控,可明显缩短种植后的炎症浸润过程加速骨愈合,使新骨矿化的效率显著提升。团队合作成果近期以“多功能金属-酚类纳米涂层在种植体上通过早期免疫调节增强骨整合(A Multifunctional Metal-Phenolic Nanocoating on Bone Implants for Enhanced Osseointegration via Early Immunomodulation)”为题,发表在国际期刊Advanced Science上,葛少华教授、李建华教授、北京大学口腔医学院韩建民教授为共同通讯作者,山东大学医学院(医院)刘金博士为第一作者。近年来,山东大学口腔医学院(口腔医院)高度重视学科交叉融合,主动对接国家战略需求,充分利用学校学科门类齐全优势,大力推进“口腔+X”团队攻关,取得了一系列交叉研究成果。葛少华、李建华教授口腔生物材料研究团队致力于新型生物材料在口腔基础医学领域的基础和应用研究,研究成果发表在Adv Funct Mater(2023)、ACS Nano (2024, 2023)、Adv Sci(2024, 2021)、Nano Energy(2024,2021)、Int J Oral Sci (2022)等。上述研究得到了国家自然科学基金、泰山学者、齐鲁青年学者、山东省重点研发计划(重大科技创新工程)等基金的支持。